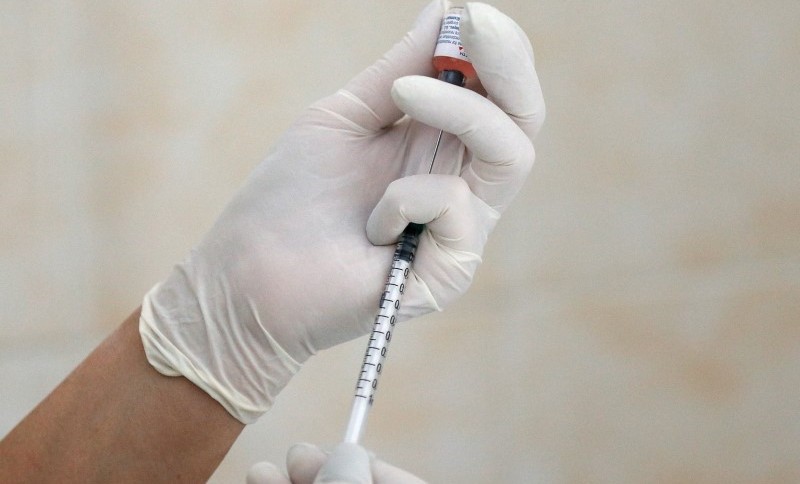
Quatro delas estão no Programa Nacional de Imunizações: Coronavac; Pfizer; AstraZeneca e Janssen; lista da OMS permite que imunizantes entrem no consórcio Covax
A Organização Mundial da Saúde (OMS) liberou nesta quarta-feira (3) a oitava vacina contra Covid-19 para uso emergencial desde o início da pandemia. A Covaxin, do laboratório indiano Bharat Biotech, entrou para a Lista de Uso Emergencial da OMS (EUL, na sigla em inglês), um pré-requisito para o fornecimento da vacina por meio do consórcio Covax, que distribui a preços de custo vacinas para países pobres e em desenvolvimento.
Desde o início da pandemia, a OMS aprovou o uso emergencial das vacinas contra Covid-19 ComiRNAaty, da Pfizer/BioNTech; a Vaxzevria da AstraZeneca/Oxford, produzidas pela AstraZeneca-SKBio (República da Coreia) e a Covishield, do Serum Institute of India; a vacina Ad26.COV2.S da Janssen; a vacina mRNA-1273 da Moderna, além das vacinas dos fabricantes chineses Sinopharm (Vero Cell) e Sinovac (Coronavac).
A Lista de Uso Emergencial da OMS também permite que os países agilizem sua própria aprovação regulatória para importar e administrar vacinas contra a Covid-19.
Além disso, os imunizantes somente entram na lista após a OMS avaliar a qualidade, segurança e eficácia das doses contra a Covid-19, bem como planos de gestão de risco e adequação programática, como requisitos de rede de frio.
No Brasil, a Agência Nacional de Vigilância Sanitária (Anvisa) já liberou o uso emergencial das vacinas Coronavac, produzida pelo Instituto Butantan; da Pfizer/BioNTech; da AstraZeneca/Oxford, produzidas pela Fundação Oswaldo Cruz (Fiocruz) e da Janssen.
A Anvisa havia votado a favor do uso emergencial da Covaxin no Brasil, mas, após escândalo envolvendo a compra da vacina pelo Ministério da Saúde, a agência reguladora voltou atrás e impediu o uso da vacina no país.
Vacinas cujo uso emergencial foi autorizado pela OMS:
- ComiRNAaty (Pfizer/BioNTech);
- Vaxzevria (AstraZeneca/Oxford/SKBio)
- Covishield (Serum Institute of India)
- COV2.S (Janssen);
- mRNA-1273 (Moderna);
- Vero Cell (Sinopharm)
- Coronavac (Sinovac)
- Covaxin (Bharat Biotech)
Entenda importância da lista de uso emergencial
O procedimento da lista avalia a adequação de novos produtos de saúde durante emergências sanitárias. O objetivo é disponibilizar medicamentos, vacinas e diagnósticos o mais rápido possível para atender à emergência, respeitando critérios rigorosos de segurança, eficácia e qualidade. A avaliação considera a ameaça representada pela emergência, bem como o benefício que resultaria do uso do produto contra quaisquer riscos potenciais.
A Lista de Uso Emergencial da OMS envolve uma avaliação rigorosa dos dados de ensaios clínicos de fase II e fase III, bem como dados adicionais substanciais sobre segurança, eficácia, qualidade e um plano de gerenciamento de risco.
Esses dados são revisados por especialistas independentes e equipes da OMS que consideram o corpo atual de evidências sobre a vacina em consideração, os planos para monitorar seu uso e os planos para estudos adicionais, diz a OMS em sua página sobre a EUL.
Como parte do processo da lista de uso emergencial, a empresa que produz a vacina deve se comprometer a continuar gerando dados para permitir o licenciamento completo e a pré-qualificação da vacina pela OMS.
O processo de pré-qualificação da OMS avaliará dados clínicos adicionais gerados a partir de testes de vacinas e implantação em uma base contínua para garantir que a vacina atenda aos padrões necessários de qualidade, segurança e eficácia para uma disponibilidade mais ampla, afirma a OMS.
FONTE: CNN BRASIL